N.S LLUVIA ACIDA
viernes, 20 de marzo de 2015
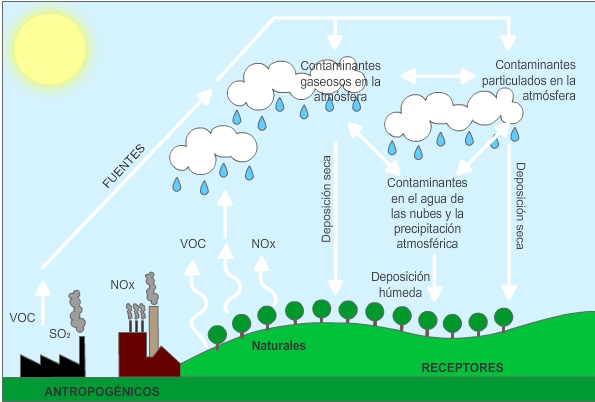
COMO SE FORMA LA LLUVIA ACIDA
La lluvia ácida se forma cuando la
humedad en el aire se combina con los óxidos de nitrógeno, el dióxido de azufre
y el trióxido de azufre emitidos por fábricas, centrales eléctricas, calderas
de calefacción y vehículos que queman carbón o productos derivados del petróleo
que contengan azufre. En interacción con el agua de la lluvia, estos gases
forman ácidos nítricos, ácido sulfuroso y ácido sulfúrico. Finalmente, estas
sustancias químicas caen a la tierra acompañando a las precipitaciones,
constituyendo la lluvia ácida.
A los seres vivos:EFECTO DE LA LLUVIA ACIDA EN LOS SERES VIVOS

Crea enfermedades respiratorias y de la piel, pero más que todo la
lluvia ácida afecta a los animales que viven en el medio acuático y en el medio
terrestre ya que al contener óxidos de azufre, entre otros, se forma al
contacto con el agua y después de una serie de reacciones ácido sulfúrico que
es el que produce esa lluvia acida
A las plantas:
La lluvia ácida no destruye directamente a las plantas y árboles,
sino que los debilita, haciéndolas vulnerables al viento, al frío, la sequía y
a los parásitos. Afecta directamente a las hojas, despojándolas de su cubierta
cerosa que le sirve de protección y provocando pequeñas lesiones que alteran el
proceso de fotosíntesis; asimismo, la lluvia ácida arrastra ciertos nutrientes
del suelo necesarios para el crecimiento.
Al ambiente:
Tiene consecuencias negativas sobre el medio ambiente, porque no
sólo afecta a la calidad del agua, sino también a los suelos, a los ecosistemas
Los efectos de la lluvia ácida sobre el terreno dependen en gran
medida del tipo de suelo sobre el que se deposita. Si el terreno es una
formación de origen calcáreo, los ácidos serán rápidamente absorbidos por el
carbonato cálcico que compone esta clase de suelos. Por el contrario, si la
superficie de depósito es de composición arcillosa o granítica, las
consecuencias son más graves, dado el enorme poder de disolución que tiene este
tipo de agua de lluvia, que acaba alterando el pH medio del terreno originando
una solidificación general. Al filtrarse en la tierra, los ácidos destruyen los
nutrientes esenciales del suelo, tales como el magnesio, el calcio y el
potasio, que alimentan a las plantas y los árboles. Estos se vuelven ralos y
descoloridos, y mueren. Otro efecto de la lluvia ácida es el aumento de la
acidez en las aguas dulces, como consecuencia del incremento de metales pesados
muy tóxicos (plomo, aluminio, mercurio, cinc y manganeso), que provocan la
ruptura de las cadenas tróficas y del proceso reproductivo de los peces,
condenando a los ríos y lagos a una lenta pero implacable disminución de su
fauna. Los lagos tienen un pH casi neutro, debido a que minerales como el calcio,
liberados en sus aguas a través del suelo, neutralizan la lluvia natural. Sin
embargo, este mecanismo amortiguador puede no ser suficiente para absorber el
incremento de acidez de aquélla
COMO SE MIDE LA ACIDEZ
Los ácidos destruyen casi todo lo que alcanzan; son solubles en agua y su fuerza se mide por el pH (potencial de nitrógeno). La escala del pH abarca valores desde 1 hasta 14. El 1 indica acidez extrema y el 7 neutralidad; el 14 se da en líquidos de gran alcalinidad (lo opuesto a la acidez). El pH se determina con un medidor especial o papel indicador. Un ácido fuerte como el sulfúrico hace que el papel se coloree de rojo, uno neutro lo pone verde, y los líquidos muy alcalinas le dan una coloración púrpura.
LIQUIDO
|
COLOR DEL INDICADOR
|
PH
|
Ácido Sulfúrico Concentrado
|
Rojo
|
1.0
|
Jugo de Limón
|
Rojo
|
2.3
|
Vinagre
|
Rosa
|
3.3
|
Lluvia Zonas Industriales
|
Rosa
|
4.3
|
Lluvia Normal
|
Naranja
|
5.5
|
Lluvia Destilada
|
Verde
|
7.0
|

LA LUCHA CONTRA LA LLUVIA ACIDA
Desde los años ochenta, se ha producido una toma de conciencia
sobre la necesidad de controlar y paliar, en la medida de lo posible, los
efectos perniciosos que sobre el medio natural ejercen las sociedades humanas.
Las inversiones se han concentrado en impulsar el desarrollo de las llamadas
energías limpias (solar y eólica, fundamentalmente), y la implantación de
controles más rigurosos para limitar la liberación a la atmósfera de agentes
contaminantes.
Los países industrializados han movilizado gran cantidad de recursos económicos para reducir las emisiones ácidas. En 1993, la UE acordó reducir las emisiones de óxidos de azufre en un 40% para el año 1998 y en un 60% para el 2003, y las de óxidos nitrosos, en un 30% para 1998. Otra de las medidas acordadas a partir del año 1993 fue la de instalar catalizadores en los coches de nueva fabricación, para conseguir la reducción de las emisiones de los mencionados gases. Uno de los progresos más significativos ha tenido lugar en las cámaras de producción de las centrales termoeléctricas, un causante esencial de las emisiones de ácidos a la atmósfera: se han incorporado técnicas que reducen e incluso eliminan la emisión de los óxidos de nitrógeno y azufre, que son recuperados y reutilizados como abono.
Suscribirse a:
Comentarios (Atom)
.jpg)


